EESTI HAIGEKASSA TERVISHOIUTEENUSTE LOETELU MUUTMISE TAOTLUS. Peeter Padrik.
|
|
|
- Jaan Nõmme
- 4 aastad tagasi
- Vaatused:
Väljavõte
1 EESTI HAIGEKASSA TERVISHOIUTEENUSTE LOETELU MUUTMISE TAOTLUS 1. Taotluse algataja Organisatsiooni või ühenduse nimi Postiaadress Eesti Onkoteraapia Ühing Puusepa 8, Ruum K4014 Telefoni- ja faksinumber ; faks: E-posti aadress Kontaktisiku ees- ja perekonnanimi ning kontaktandmed Peeter Padrik 2. Teenuse nimetus, kood ja kohaldamise tingimus(ed) 2.1. Teenuse nimetus Neerukasvajate kemoteraapiakuur, ravimi nivolumab lisamine olemasolevatele ravidele 2.2. Teenuse kood tervishoiuteenuste loetelus (edaspidi loetelu) olemasoleva teenuse korral 352R 2.3. Kohaldamise tingimus(ed) Võimalik on uus ravimikomponent lisada olemasolevasse komplekshinda või täiendavalt eraldi hinnana Ettepaneku eesmärk Uue tervishoiuteenuse (edaspidi teenuse) lisamine loetellu 1 X Loetelus olemasoleva teenuse piirhinna muutmine 2 Teenuse kohaldamise tingimuste muutmine 3 Teenuse nimetuse muutmine 4 Teenuse kustutamine loetelust 5 Teenuse omaosaluse määra muutmine 6 Muu (selgitada) 1 Täidetakse kõik taotluse väljad või tuuakse selgitus iga mittetäidetava välja kohta, miks seda ei ole võimalik/vajalik täita. 2 Kui teenuse piirhinna muutmise tingib uue meditsiiniseadme, ravimi vm lisamine teenuse kirjeldusse, täidetakse taotluses uue ressursi kohta kõik väljad või tuuakse selgitus iga vastava mittetäidetava välja juurde, miks seda ei ole võimalik/vajalik täita. Kui piirhinna muutmise tingib ressursi maksumuse muutus, täidetakse vähemalt väljad 1-3 ning Täidetakse kõik allpool esitatud väljad või tuuakse selgitus iga vastava mittetäidetava välja kohta, miks seda ei ole võimalik/vajalik täita. 4 Täidetakse punktid 1-3 ning esitatakse vaba tekstina põhjendus teenuse nimetuse muutmise vajalikkuse kohta. 5 Täidetakse taotluse punktid 1-3 ning esitatakse vaba tekstina põhjendus teenuse kustutamise kohta. 6 Täidetakse punktid 1-3, 7, 11 ning esitatakse vaba tekstina põhjendus omaosaluse muutmise kohta. Lk 1 / 13
2 2.5. Peatükk loetelus, kus teenus peaks sisalduma Üldarstiabi Ambulatoorne eriarstiabi Meditsiiniseadmed ja ravimid Statsionaarne eriarstiabi Uuringud ja protseduurid Operatsioonid Laboriuuringud, lahangud ja kudede transplantaadid Veretooted ja protseduurid veretoodetega Hambaravi Kompleksteenused Ei oska määrata/ Muu (selgitada) 3. Tõenduspõhisus ja näidustused 3.1. teenuse osutamise meditsiinilised näidustused ja vajadus teenuse osutamiseks; Neerukasvajate kemoteraapiakuuri (kood 352R) teenus sisaldab praegu järgmisi raviskeeme: 1) bevacizumabravi: kaugelearenenud heledarakulise neeruvähi 1. rea ravi madala ja keskmise riskiga patsiendil kombinatsioonis interferoon alfaga; 2) temsirolimuse monoravi: kaugelearenenud heledarakulise neeruvähi 1. rea ravi kõrge riskiga patsiendil. Lisaks on retseptiravimitena Eesti Haigekassa ravimite loetelus: Sunitiniib: IV staadiumis heledarakulise neeru kartsinoomi esimese rea ravina vo i teise rea ravina pa rast interferooni sisaldava ravi ebao nnestumist patsientidele, kellel ravi alustamine ja ja tkamine sunitiniibiga on hinnatud konsiiliumi (va hemalt kahe onkoloogi) poolt vastavaks ja rgmistele kriteeriumidele: patsiendi u ldseisund ECOG kriteeriumide ja rgi on 0-1, haiguse prognoos Hengi kriteeriumide ja rgi hea vo i keskmine ning mitte enam kui 3 ravikuu mo o dumisel on saavutatud ta ielik vo i osaline ravivastus vo i haigus pu sib stabiilsena Pasopaniib: IV staadiumis heledarakulise neeru kartsinoomi esimese rea ravina vo i teise rea ravina pa rast interferooni sisaldava ravi ebao nnestumist patsientidele, kellel ravi alustamine ja ja tkamine pasopaniibiga on hinnatud konsiiliumi (va hemalt kahe onkoloogi) poolt vastavaks ja rgmistele kriteeriumidele: patsiendi u ldseisund ECOG kriteeriumide ja rgi on 0-1, haiguse prognoos Hengi kriteeriumide ja rgi hea vo i keskmine ning mitte enam kui 3 ravikuu mo o dumisel on saavutatud ta ielik vo i osaline ravivastus vo i haigus pu sib stabiilsena. Aksitiniib: IV staadiumis heledarakulise neeru kartsinoomi teise rea ravina pa rast esimese rea sunitiniib- vo i pasopaniibravi patsientidele, kellel ravi alustamine ja ja tkamine aksitiniibiga on hinnatud konsiiliumi (va hemalt kahe onkoloogi) poolt vastavaks ja rgmistele kriteeriumidele: patsiendi u ldseisund ECOG kriteeriumide ja rgi on 0-1, haiguse prognoos Hengi kriteeriumide ja rgi hea vo i keskmine ning mitte enam kui 3 ravikuu mo o dumisel on saavutatud ta ielik vo i osaline ravivastus vo i haigus pu sib stabiilsena Sorafeniib: IV staadiumis heledarakulise neeru kartsinoomi teise rea ravina pa rast interferooni sisaldava ravi ebao nnestumist patsientidele, kellel ravi alustamine ja ja tkamine sorafeniibiga on hinnatud konsiiliumi (va hemalt kahe onkoloogi) poolt vastavaks ja rgmistele kriteeriumidele: patsiendi u ldseisund ECOG kriteeriumide ja rgi on 0-1, haiguse prognoos Hengi kriteeriumide ja rgi hea vo i keskmine ning mitte enam kui 3 ravikuu mo o dumisel on saavutatud ta ielik vo i osaline ravivastus vo i haigus pu sib stabiilsena. Lk 2 / 13
3 Seega on sisuliselt praegu kaetud kahe ravirea ravi, kuid praegune ravikompleks pole piisavalt efektiivne: valdaval enamikul patsientidel progresseerub metastaatiline haigus mingil raviperioodil, osadel patsientidel esineb talumatus olemasoleva ravi osas. Seega on olemas selge vajadus metastaatilise neeruvähi täiendavateks ravivõimalusteks. Taotleme ravimi nivolumab lisamist metastaatilise neeruvähi ravikompleksi. Nivolumabi monoteraapia on näidustatud kaugelearenenud neerurakk-kartsinoomi raviks täiskasvanutel eelneva ravi järgselt. Nivolumab on uudne kasvajavastane immuunravi. Nivolumab on inimese immuunglobuliin G4 (IgG4) tüüpi monoklonaalne antikeha (HuMAb), mis seondub PD-1 (programmed death-1, programmeeritud rakusurm 1) retseptori külge ja blokeerib selle ühinemise PD-L1 ja PD-L2-ga. PD-1 retseptor on T-rakkude aktiivsuse negatiivne regulaator, mille puhul on näidatud, et see osaleb T-rakulise immuunvastuse kontrollis. PD-1 seondumine ligandide PD-L1 ja PD-L2-ga, mis on ekspresseeritud antigeeni esitlevatel rakkudel ja mida võivad ekspresseerida kasvajad või teised rakud kasvaja mikrokeskkonnas, annab tulemuseks T-rakkude proliferatsiooni ja tsütokiinide sekretsiooni. Nivolumab potentseerib T-rakulist immuunvastust, sealhulgas kasvajavastaseid reaktsioone blokeerides PD-1 seondumise PD-L1 ja PD-L2 ligandidega teenuse tõenduspõhisus avaldatud kliiniliste uuringute alusel taotletud näidustuste lõikes; Randomiseeritud III faasi avatud uuringus (CA209025) hinnati 3 mg/kg nivolumabi monoteraapia ohutust ja efektiivsust heledarakulise kaugelearenenud neerurakk-kartsinoomi korral (1). Uuringusse kaasati (18-aastased ja vanemad) patsiendid, kelle haigus oli progresseerunud ühe või kahe varasema antiangiogeense raviskeemi kasutamise ajal või pärast seda ning kes ei olnud eelnevalt saanud kokku üle kolme süsteemse raviskeemi. Patsientidel pidi olema Karnofsky sooritusvo ime skoor (KPS) 70%. Patsiendid kaasati uuringusse sõltumata nende tuumori PD-L1 staatusest. Uuringust jäeti välja patsiendid, kellel olid anamneesis või esinesid samaaegselt ajumetastaasid, kes olid eelnevalt saanud ravi imetaja rapamütsiinimärklaua (mtor) inhibiitoriga, kellel oli aktiivne autoimmuunhaigus või haigusseisundid, mis vajasid süsteemset ravi immunosupressantidega. Kokku 821 patsienti randomiseeriti saama kas 3 mg/kg nivolumabi (n = 410), manustatuna intravenoosselt 60 minuti jooksul iga 2 nädala järel, või everoliimust (n = 411) 10 mg ööpäevas, manustatuna suu kaudu. Ravi jätkati seni, kuni täheldati kliinilist kasu, või kuni patsient enam ravi ei talunud. Esimesed kasvaja hindamised tehti 8 nädalat pärast randomiseerimist ja need jätkusid iga 8 nädala järel esimesel aastal ja seejärel iga 12 nädala järel kuni haiguse progresseerumise või ravi lõpetamiseni, ükskõik kumb saabus varem. Kasvaja hindamisi jätkati pärast ravi lõpetamist patsientidel, kes lõpetasid ravi muudel põhjustel kui haiguse progresseerumine. Pärast esialgset uurija poolt hinnatud RECIST versiooni 1.1 kriteeriumidel põhinevat haiguse progresseerumist oli ravi lubatud juhul, kui täheldati kliinilist kasu ja uuringuravim oli uurija hinnangul patsiendi poolt talutav. Esmane efektiivsuse tulemusnäitaja oli OS. Teisesed tulemusnäitajad olid uurija poolt hinnatud ORR ja PFS. Ravieelsed näitajad olid kahe rühma vahel üldiselt tasakaalus. Enamik patsientidest (72%) olid eelnevalt saanud ühte antiangiogeenset ravi. Pärast haiguse progresseerumist jätkas nivolumabi harus ravi nivolumabiga 44% patsientidest ja 46% patsientidest everolimusega everolimuse harus. Lk 3 / 13
4 Jr k nr. Uurin gu autori( te) nimed Uurin gu kvalite et 7 Uuringusse hõlmatud isikute arv ja lühiiseloom ustus Uuritava teenuse kirjeldus Esma ne tulem us, mida hinna ti Muu(d) tulemus(ed), mida mõõdeti/ hinnati Alternatii v(id) millega võrreldi Motzer RJ, et al. (1) B Kokku 821 patsient i, nivolumabi grupis n = 410, versus everoliimus e grupis n = 411. Uuringusse kaasati (18-aastase d ja vanemad) patsiendid, kelle haigus oli progresseer unud ühe või kahe varasema antiangioge ense raviskeemi kasutamise ajal või pärast seda ning kes ei olnud eelnevalt saanud 3 mg/kg nivolumab i manustatu na intravenoo sselt 60 minuti jooksul iga 2 näda la järel Üldin e elule mus (over all surviv al OS) Üldine ravivastus(ov erall response rate, ORR) ja progressioon ivaba elulemus (progressioo n free survival, PFS) Everoliim us 10 mg ööpäevas, manustatu na suu kaudu. Jälgim ise perio d Jälgitu d 398 juhtu 7 Märgitakse järgmiselt: A tugevalt tõenduspõhine (põhineb süstemaatilisel ülevaatel kõigist asjakohastest randomiseeritud kliinilistest uuringutest ja/või metaanalüüsil); B tõenduspõhine (põhineb vähemalt ühel korralikult disainitud randomiseeritud kliinilisel uuringul), C kaheldav või nõrgalt tõenduspõhine (juhul, kui pole A ega B, aga tõenduspõhisus on kirjeldatud kirjanduse põhjal); D muu, selgitada. Lk 4 / 13
5 kokku üle kolme süsteemse raviskeemi. Patsientidel pidi olema Karnofsky sooritusvõi me skoor (KPS) 70% teenuse sisaldumine punktis 3.1 esitatud näidustustel Euroopa riikides aktsepteeritud ravijuhistes; European Society for Medical Oncology (ESMO) neeruvähi ravijuhendi kohaselt on nivolumab metastaatilise neeruvähi standardravi türosiinkinaasi inhibiitorravi järgselt ühe või kahe ravirea järgselt (2). Sealjuures on väljatoodud tõenduspõhisus tugevam 2. rea ravina (IA) võrreldes 3. reaga (IIA). ESMO kliinilise kasu skaala (ESMO-Magnitude of Clinical Benefit Scale) järgi on nivolumab hinnatud kõige tugevama skooriga 5. Tartu Ülikooli Kliinikumi vähikeskuse neeruvähi ravijuhis JKL versioon 01 sätestab metastaatilise neeruvähi ravi praegu järgnevalt (ka PERH ja Ida-Tallinna Keskhaigla järgivad samu põhimõtteid): 2.2. Metastaseerunud haiguse ravi Tsütoreduktiivne nefrektoomia heas üldseisundis ulatusliku algkoldega patsientidel, samuti sümptomaatilise algkoldega patsientidel Metastaaside kirurgiline eemaldamine nende potentsiaalse resetseeritavuse korral Süsteemne ravi: a) Helerakk-kartsinoom, hea või keskmine prognoos 1. rea ravi: sunitiniib või pasopaniib või interferoon-alfa + bevacizumab ravivalik sõltub patsiendi kaasuvatest patoloogiatest, metastaaside paikmest, patsiendi eelistustest tervikliku raviplaani osas. 2. rea ravi: interferoonravi järgselt pasopaniib, sunitiniib või sorafeniib; türosiinkinaasi inhibiitorravi järgselt: aksitiniib; 3. rea ravi: everolimus (ei ole Eesti Haigekassa poolt rahastatud). nivolumab (ei ole Eesti Haigekassa poolt rahastatud; on olnud võimalik taotleda Bristol Myers Squibb laiendatud kättesaadavuse programmi raames). b) Helerakk-kartsinoom, halb prognoos temsirolimus või parim toetav ravi. Alternatiivne ravivõimalus on sunitiniib (ei ole halva riskigrupi korral Eesti Haigekassa poolt rahastatud). c) Mitte-helerakk-kartsinoom temsirolimus Rahastamise korral võiks nivolumab lisanduda ühe nii 2. kui ka 3. ravirea võimalusena. Lk 5 / 13
6 3.4. teenuse osutamise kogemus maailmapraktikas ja Eestis punktis 3.1 esitatud näidustuste lõikes; Maailmapraktikat kajastab kõige paremini eelpool väljatoodud III faasi kliiniline uuring (1). Nivolumab on saanud maailmas metastaatilise neeruvähi standardravi kompleksi üheks osaks. Eestis on kasutatud nivolumabi metastaatilise neeruvähi korral laiendatud kättesaadavuse programmi raames, mis andnud mitmele patsiendile pikaajalised püsivad ravivastused, nendel patsientidel ravi jätkub programmi raames, kuid uutele patsientidele on ravi kättesaadavus alates aastast lõppenud aastal on saanud laiendatud kättesaadavuse programmi raames ravi nivolumabiga 21 metastaatilise neeruvähi patsienti (TÜK 9 patsienti, PERH, 11 patsienti ja ITK 1 patsient) Meditsiinilise tõenduspõhisuse võrdlus Eestis ja rahvusvaheliselt kasutatavate alternatiivsete tervishoiuteenuste, ravimite jm. Eestis ravialternatiivi ei ole, sest võimalik alternatiiv everolimuse näol pole Haigekassa poolt rahastatud. Seega on patsientidele võimalik praegu rakendada pärast kaht rida türosiinkinaasinhibiitorravi vaid edasist sümptomaatilist ravi. Arvestades, et everolimuse uuring võrreldes platseeboga näitas haiguse progressioonivaba elulemuse paranemist 4,9 [95% CI ] versus 1,9 [ ] kuud (3), saame väita, et nivolumab annaks Eesti metastaatilise neeruvähiga patsientidele türosiinkinaasinhibiitorravi järgselt nii üldise (25,0 kuud nivolumabiga versus 19,6 kuud everolimusega) kui ka progressioonivaba elulemuse paranemise. Otsene nivolumabi võrdlus Eestis standardiks oleva sümptomaatilise raviga puudub, mistõttu oleks efekt Eesti haigetele kliiniliste uuringute tulemusega võrreldes ilmselt veel suurem teenuse seos kehtiva loeteluga, sh uue teenuse asendav ja täiendav mõju kehtivale loetelule; Lisandub neeruvähi komplekshinda 352R või rakendatakse eraldi komplekshinnana teenuse seos erinevate erialade ja teenuse tüüpidega; Teenus on seotud onkoloogia erialaga ja ambulatoorse raviteenusena. 4. Teenusest saadav tulemus ja kõrvaltoimed 4.1. teenuse oodatavad ravitulemused ning nende võrdlus punktis 3.2 esitatud alternatiividega (ravi tulemuslikkuse lühi- ja pikaajaline prognoos): Randomiseeritud III faasi avatud uuringus (CA209025) näidati üldise elulemuse statistiliselt olulist paranemist nivolumabi saanud randomiseeritud patsientidel everolimusega võrreldes eelnevalt kavandatud vaheanalüüsi põhjal, mis viidi läbi siis, kui oli jälgitud 398 juhtu (70% lõplikuks analüüsiks kavandatud juhtude arvust). Paremaid üldise elulemuse tulemusi täheldati vaatamata tuumori PD-L1 ekspressiooni tasemele. Üldise elulemuse Kaplan-Meieri kõverad on esitatud joonisel 1. Lk 6 / 13
7 Joonis 1: Üldise elulemuse Kaplan-Meieri kõverad (CA209025) Elulemuse tõenäosus Üldine elulemus (kuudes) Riskipatsientide arv Nivolumab Everoliimus Nivolumab 3 mg/kg (juhtusid: 183/410), mediaan ja 95% CI: 25,00 (21,75; N.A.) Everoliimus 10 mg (juhtusid: 215/411), mediaan ja 95% CI: 19,55 (17,64; 23,06) Efektiivsuse tulemused on toodud tabelis 1. Tabel 1: Efektiivsuse tulemused (CA209025) Taotletavast teenusest saadav tulemus: nivolumab (n = 410) Võrdlusgrupp uuringus: everoliimus (n = 411) Üldine elulemus Juhud 183 (45) 215 (52) Riskide suhe 0,73 98,52% CI (0,57; 0,93) p-väärtus 0,0018 Mediaan (95% CI) 25,0 (21,7; NE) 19,6 (17,6; 23,1) Lk 7 / 13
8 Määr (95% CI): 6. kuul 89,2 (85,7; 91,8) 81,2 (77,0; 84,7) 12. kuul 76,0 (71,5; 79,9) 66,7 (61,8; 71,0)) Objektiivne ravivastus 103 (25,1%) 22 (5,4%) (95% CI) (21,0; 29,6) (3,4; 8,0) Šansside suhe (95% CI) 5,98 (3,68; 9,72) p-väärtus < 0,0001 Täielik ravivastus (CR) 4 (1,0%) 2 (0,5%) Osaline ravivastus (PR) 99 (24,1%) 20 (4,9%) Stabiilne haigus (SD) 141 (34,4%) 227 (55,2%) Progressioonivaba elulemus Juhud 318 (77,6) 322 (78,3) Riskide suhe 0,88 95% CI (0,75; 1,03) p-väärtus 0,1135 Mediaan (95% CI) 4,6 (3,71; 5,39) 4,4 (3,71; 5,52) + ta histab tsenseeritud vaatlust. NE = mittehinnatav Surma riskimäära vähenemine nivolumab-raviga võrreldes everolimusega oli 0,73 (98.5% CI, 0,57 kuni 0,93; P=0,002), mis vastas eelnevalt seatud paremuse kriteeriumile (P 0,0148). Objektiivse ravivastuse saavutamiseks kulunud ajavahemiku mediaan olid 3,5 kuud (vahemik: 1,4...24,8 kuud) pärast nivolumabiga ravi alustamist. Neljakümne üheksal (47,6%) ravile reageerinud patsiendil püsis ravivastus kestusega vahemikus 0,0...27,6 + kuud. Üldise elulemusega võib kaasneda haigusega seotud sümptomite ja mitte-haigusspetsiifilise elukvaliteedi (QoL) paranemine aja jooksul, mille hindamiseks kasutati valiidseid ja usaldusväärseid FKSI-DRS (Assessment of Cancer Therapy-Kidney Symptom Index-Disease Related Symptoms, vähiravi hindamineneerusümptomite indeks-haigusega seotud sümptomid) ja EuroQoL EQ-5D skaalasid. Selgelt märkimisväärne sümptomite paranemine (MID=FKSI-DRS skoori 2-punktiline muutus; p 0,001) ja paranemiseni kulunud aeg (HR = 1,66 (1,33;2,08), p < 0,001) olid oluliselt paremad nivolumabi rühma patsientidel. Kuna mõlemad Lk 8 / 13
9 uuringurühmad said aktiivset ravi, tuleb elukvaliteedi andmeid tõlgendada avatud uuringu ülesehituse kontekstis ja seetõttu ettevaatusega teenuse kõrvaltoimed ja tüsistused, nende võrdlus punktis 3.2 esitatud alternatiivide kõrvaltoimetega: Raviga seotud kõrvaltoimeid esines 79 %-l patsientidest nivolumabi grupis ja 88 %-l everolimuse grupis. Tõsiseid, 3. Ja 4. astme kõrvaltoimeid esines 19 %-l nivomulabi saanud patsientidest ja 37 % everolimust saanud patsientidest. Kõige sagedasem kõrvaltoime nivolumabiga oli nõrkus (2 %) ja kõige sagedasem everolimusega oli aneemia (8 %). Enamlevinud kõrvaltoimed on toodud ära järgnevas tabelis 2. Tabel 2. Enamlevinud kõrvaltoimed. P 3.2. tabeli uuringu jrk nr. Teenuse kõrvaltoimed ja tüsistused Taotletav teenus Nivolumab Everolimus Kõik, % Aste, % Kõik, % Aste, % 1 Kõik Nõrkus Iiveldus 14 alla Sügelus Diarröa Isu langus 12 alla Naha punetus 10 alla Köha Aneemia Düspnoe Pneumoniit Mukoosa põletik punktis 4.2. ja 3.5 esitatud kõrvaltoimete ja tüsistuste ravi kirjeldus (kasutatavad tervishoiuteenused ja/või ravimid (k.a ambulatoorsed ravimid)); Raviga saadav kasu ületab tüsistuste riski. Immuunvastust stimuleeriva ravina ei kaasne nivolumabiga tüüpilised tsütostaatilise ravi kõrvaltoimed, samas võivad sellega kaasneda immuunsüsteemi vahendatud reaktsioonid (nahalööbed, kõhulahtisus, harvem ka pneumoniit, hepatiit, endokrinopaatiad jms), mis on üldjuhul ravitavad glükokortikosteroididega. Erihoiatused ja ettevaatusabinõud ravimi kasutamisel, samuti soovitused ravi modifitseerimiseks on toodud ära nivolumabi ravimi omaduste kokkuvõttes: _Product_Information/human/003985/WC pdf Immuunsüsteemiga seotud kõrvaltoimete käsitlemiseks on välja töötatud Euroopa Ravimiameti poolt heaks kiidetud juhised, mis on leitavad Ravimiameti kodulehelt: Taotletava teenuse osutamiseks ja patsiendi edasiseks jälgimiseks vajalikud tervishoiuteenused ja ravimid (s.h ambulatoorsed) vm ühe isiku kohta kuni vajaduse lõppemiseni ning võrdlus punktis 3.5 nimetatud alternatiividega kaasnevate teenustega; Lk 9 / 13
10 Täiendavad teenused ja ravimid ei ole vajalikud teenuse võimalik väär-, ala- ja liigkasutamine; teenuse optimaalse ja ohutu kasutamise tagamiseks teenusele kohaldamise tingimuste seadmise vajalikkus; Ravi näidustused ja vastunäidustused on selgelt defineeritud ravimi omaduste kokkuvõttes: _Product_Information/human/003985/WC pdf Teenust osutab kvalifitseeritud onkoloogilisele ravile spetsialiseerunud personal, kes on pädev bioloogilise ravi ja ravitüsistuse kõikides üksikasjades ning see tagab teenuse optimaalse ja õige kasutamise patsiendi isikupära võimalik mõju ravi tulemustele; Patsiendi isikupära praeguste teadmiste valguses ravitulemust ei mõjuta, Uuringus CA ei seostunud ravivastus PD-1L ekspressiooni tasemega ning saavutatud ravitulemus pole olnud statistiliselt seostatav ka muude võimalike markeritega. Lapsed Nivolumabi ohutus ja efektiivsus lastel vanuses alla 18 aastat ei ole tõestatud. Andmed puuduvad. Eakad Eakatel ( 65-aastastel) patsientidel ei ole annuse kohandamine vajalik. Neerurakk-kartsinoomi olulisest uuringust jäeti välja patsiendid, kellel olid anamneesis või esinesid samaaegselt ajumetastaasid, aktiivne autoimmuunhaigus või süsteemset immunosupressantravi vajavad haigusseisundid. 5. Vajadus 5.1. Eestis teenust vajavate patsientide arvu hinnang (ühe aasta kohta 4 aasta lõikes), kellele on reaalselt võimalik teenust osutada taotletud näidustuste lõikes: Teenuse näidustus Patsientide arv Patsientide arv Patsientide arv Patsientide arv aastal t+3 aastal t 2018 aastal t aastal t Metastaatilise neeruvähi 2. ja 3. ravirea ravi *t taotluse menetlemise aastale järgnev aasta; Nivolumab ravi vajavate patsientide täpsem arv võiks tulla aasta statistikast Eesti Haigekassa andmebaasi alusel: neeruvähi diagnoosiga patsientide arv, kes on saanud ravi sunitiniibi, pasopaniibi, aksitiniibi või sorafeniibiga. Taotlejal vastavad andmed hetkel kogu 2016.a. kohta puuduvad. Eesti Haigekassa andmete põhjal on aasta I-III kvartalis saanud ravi aksitiniibiga 46 ja sorafenibiga 3, patsienti, kes oleks nimetatud ravimite näidustuste alusel metastaatilise neeruvähi 2. ravirea kontingent. Oma Lk 10 / 13
11 spetsiifika poolest aga ei pruugi ravi nivolumabiga olla kõigile neile sobiv (nt kaasuvad haigused) või on vastunäidustatud aastal on saanud laiendatud kättesaadavuse programmi raames Eestis ravi nivolumabiga 21 metastaatilise neeruvähi patsienti. Programmile seatud haigete sobivuskriteeriumid olid sarnased CA uuringu sobivuskriteeriumitega ja Euroopa Ravimiameti poolt nivolumabi kinnitatud näidustuse ning ka käesolevas taotluses välja toodud sobivuskriteeriumitega nivolumabi kasutamiseks taotletava tervishoiuteenuse raames, seega võiks esimese raviaasta patsientide arvuks prognoosida 25 patsienti, patsientide arv kasvaks ilmselt 2-3 patsiendi kaupa aastas teenuse mahu prognoos ühe aasta kohta 4 järgneva aasta kohta näidustuste lõikes: Kliinilises uuringus CA oli nivolumabi ravikestuse mediaan 5,5 kuud ehk ligikaudu 12 ravikuuri, seega olulist ravide kumuleerumist aastati oodata ei ole. Teenuse mahu prognoos aastati: 2018: 25 patsienti x 12 ravikuuri = 300 ravikuuri 2019: 28 patsienti x 12 ravikuuri = 336 ravikuuri 2020: 30 patsienti x 12 ravikuuri = 360 ravikuuri 2021: 33 patsienti x 12 ravikuuri = 396 ravikuuri 6. Taotletava teenuse kirjeldus 6.1. teenuse osutamiseks vajalik koht (palat, protseduuride tuba, operatsioonituba, vm); Intravenoosne manustamine ambulatoorse keemiaravi üksuses patsiendi ettevalmistamine ja selleks vajalikud toimingud: premedikatsioon, desinfektsioon või muu; Ravimi ettevalmistus haiglaapteegis vastavalt ravimi juhistele. Intravenoosne infusioon 1 tunni jooksul teenuse osutamise kirjeldus tegevuste lõikes; Nivolumabi soovitatav annus on 3 mg/kg nivolumabi, manustatuna veenisiseselt 60 minuti jooksul iga 2 nädala järel. Ravi nivolumabiga tuleb jätkata seni, kuni täheldatakse kliinilist kasu, või kuni patsient enam ravi ei talu. 7. Nõuded teenuse osutajale 7.1. teenuse osutaja (regionaalhaigla, keskhaigla, üldhaigla, perearst, vm); Raviteenust võib osutada raviasutus, kus on spetsialiseeritud onkoloogia (onkoteraapia) osakond, milles on lubatud tsütostaatiliste ravimite kasutamine. Eestis oleks võimalik praegu käesolevat raviteenust osutada kolmes raviasutuses: SA Tartu Ülikooli Kliinikum Hematoloogia-onkoloogia kliinik; SA Põhja Eesti Regionaalhaigla Onkoloogia-ja hematoloogiakliinik. AS Ida-Tallinna Keskhaigla Onkoloogiakeskus 7.2. infrastruktuur, tervishoiuteenuse osutaja täiendavate osakondade/teenistuste olemasolu vajadus; On olemas personali (täiendava) väljaõppe vajadus; Ei ole. Ravi peab läbi viima onkoloog. Lk 11 / 13
12 7.4. minimaalsed teenuse osutamise mahud kvaliteetse teenuse osutamise tagamiseks; Kvaliteetne teenus on Eestis tagatud olemasolevate onkoloogia ambulatoorset ja statsionaarset tegevusluba omavate raviasutuste baasil teenuse osutaja valmisoleku võimalik mõju ravi tulemustele. Ei ole. Ravi peab läbi viima vastava kogemusega onkoloog. 8. Kulutõhusus 8.1. teenuse hind; hinna põhjendus/selgitused; Meile teadaolevalt on nivolumabi hulgimüügi ostuhind koos võimaliku allahindlusega ning sellele vastav hulgimüügi väljamüügihind maksimaalse lubatud juurdehindluse korral: Nivolumab 40 mg: xxx EUR ilma käibemaksuta, hind haiglale käibemaksuga xxx EUR. Nivolumab 100 mg: xxx EUR ilma käimamaksuta, hind haiglale käibemaksuga xxx EUR. Seega on keskmise 80 kg patsiendi jaoks vajalik ravimikogus 240 mg, ravikuuri maksumus kokku xxx EUR. 40 mg ja 100 mg viaalide kombineerimisel on nivolumabi võimalik annustada täpsusega 20 mg (vastab 3,3 kg kehakaalule), seega on ravimikadu minimaalne. Lisaks on haiglaapteekides võimalik jagada viaale patsientide vahel kui erinevate patsientide ravikuurid on samal või järjestikustel päevadel, mis omakorda vähendab ravimikadu. Uuringus CA oli ravikestuse mediaan 5,5 kuud ehk ligikaudu 12 ravikuuri kogumaksumusega xxxx EUR. Kulutõhususe kalkulatsioonide ning Haigekassa eelarvemõjude analüüsimiseks palume kontakteeruda ravimitootja BMS Eesti esindaja Amicus Pharma ga Loodame, et Eesti jaoks on tootjal võimalus pakkuda kulu- ja/ või riskijagamise skeeme teenuse osutamisega kaasnevate teenuste ja soodusravimite, mis on nimetatud p 4.4, isiku kohta kuni vajaduse lõppemiseni esitatud kulude võrdlus alternatiivsete teenuste kuludega isiku kohta kuni vajaduse lõppemiseni; Puudub ajutise töövõimetuse hüvitise kulude muutus ühe raviepisoodi kohta tuginedes tõenduspõhistele uuringutele võrreldes alternatiivsete teenustega; Kulutused ajutise töövõimetuse kompenseerimiseks võivad väheneda tulenevalt ravi efektiivsusest ja keemiaraviga võrreldes leebest kõrvaltoimete profiilist patsiendi poolt tehtavad kulutused võrreldes alternatiivsete teenuste korral tehtavate kuludega. Ei ole. 9. Omaosalus 9.1. hinnang patsientide valmisolekule tasuda ise teenuse eest osaliselt või täielikult Arvestades haiguse mõju inimese sotsiaalsele ja tervislikule seisundile ning töövõimele, ei ole omavastutus põhjendatud. Lk 12 / 13
13 10. Esitamise kuupäev Esitaja nimi ja allkiri Peeter Padrik /allkirjastatud digitaalselt 12. Kasutatud kirjandus 1. Motzer RJ, Escudier B, McDermott DF, George S, Hammers HJ, Srinivas S, et al. Nivolumab versus Everolimus in Advanced Renal-Cell Carcinoma. N Engl J Med. 2015;373(19): Escudier B, Porta C, Schmidinger M, Rioux-Leclercq N, Bex A, Khoo V, et al. Renal cell carcinoma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2016;27(suppl 5):v58-v Motzer RJ, Escudier B, Oudard S, Hutson TE, Porta C, Bracarda S, et al. Phase 3 trial of everolimus for metastatic renal cell carcinoma : final results and analysis of prognostic factors. Cancer. 2010;116(18): Lk 13 / 13
II lisa Ravimi omaduste kokkuvõtte ja pakendi infolehe muudatused, esitatud Euroopa Ravimiameti poolt Käesolev ravimi omaduste kokkuvõte ja pakendi in
 II lisa Ravimi omaduste kokkuvõtte ja pakendi infolehe muudatused, esitatud Euroopa Ravimiameti poolt Käesolev ravimi omaduste kokkuvõte ja pakendi infoleht on esildismenetluse tulemus. Vastavalt vajadusele
II lisa Ravimi omaduste kokkuvõtte ja pakendi infolehe muudatused, esitatud Euroopa Ravimiameti poolt Käesolev ravimi omaduste kokkuvõte ja pakendi infoleht on esildismenetluse tulemus. Vastavalt vajadusele
Sotsiaalministri 17. septembri a määrus nr 53 Tervise infosüsteemi edastatavate dokumentide andmekoosseisud ning nende säilitamise tingimused ja
 Sotsiaalministri 17. septembri 2008. a määrus nr 53 Tervise infosüsteemi edastatavate dokumentide andmekoosseisud ning nende säilitamise tingimused ja kord Lisa 2 Statsionaarse epikriisi andmekoosseis
Sotsiaalministri 17. septembri 2008. a määrus nr 53 Tervise infosüsteemi edastatavate dokumentide andmekoosseisud ning nende säilitamise tingimused ja kord Lisa 2 Statsionaarse epikriisi andmekoosseis
Non-pharmacological treatment
 Siinusrütmi säilitava ravimi valik Kliiniline küsimus Kas siinusrütmi säilitavaks raviks tuleks eelistada mõnd konkreetset ravimirühma/ravimit: BBL vs Ic vs III? Olulised tulemusnäitajad Surm, ajuinfarkt,
Siinusrütmi säilitava ravimi valik Kliiniline küsimus Kas siinusrütmi säilitavaks raviks tuleks eelistada mõnd konkreetset ravimirühma/ravimit: BBL vs Ic vs III? Olulised tulemusnäitajad Surm, ajuinfarkt,
Traneksaam_ortopeedias
 Traneksaamhape kasutamine Juri Karjagin Tartu Ülikool Tartu Ülikooli Kliinikum Plaan Fibrinolüüsist Traneksaamhape farmakoloogiast Traneksaamhape uuringud Plaaniline kirurgia Erakorraline trauma Toopiline
Traneksaamhape kasutamine Juri Karjagin Tartu Ülikool Tartu Ülikooli Kliinikum Plaan Fibrinolüüsist Traneksaamhape farmakoloogiast Traneksaamhape uuringud Plaaniline kirurgia Erakorraline trauma Toopiline
Pealkiri
 Elanike hinnangud arstiabile 2014, peamised arengud ja edasised tegevused Tanel Ross Haigekassa juhatuse esimees Üldised järeldused elanike hinnangutest Hinnangud Eesti tervishoiusüsteemile on püsinud
Elanike hinnangud arstiabile 2014, peamised arengud ja edasised tegevused Tanel Ross Haigekassa juhatuse esimees Üldised järeldused elanike hinnangutest Hinnangud Eesti tervishoiusüsteemile on püsinud
4. KIRURGIA Üliõpilase andmed. Need väljad täidab üliõpilane Praktikatsükli sooritamise aeg Kirurgia praktikatsükkel Ees- ja perekonnanimi Matriklinum
 4. KIRURGIA Üliõpilase andmed. Need väljad täidab üliõpilane Praktikatsükli sooritamise aeg Kirurgia praktikatsükkel Ees- ja perekonnanimi Matriklinumber E-posti aadress Telefoninumber Praktikatsükli läbimine.
4. KIRURGIA Üliõpilase andmed. Need väljad täidab üliõpilane Praktikatsükli sooritamise aeg Kirurgia praktikatsükkel Ees- ja perekonnanimi Matriklinumber E-posti aadress Telefoninumber Praktikatsükli läbimine.
KEYTRUDA (pembrolizumab) teatmik Teave patsiendile Teave patsiendile Käesoleva ravimi suhtes kohaldatakse täiendavat järelevalvet, mis võimaldab kiire
 KEYTRUDA (pembrolizumab) teatmik Teave patsiendile Teave patsiendile Käesoleva ravimi suhtes kohaldatakse täiendavat järelevalvet, mis võimaldab kiiresti tuvastada uut ohutusteavet. Te saate sellele kaasa
KEYTRUDA (pembrolizumab) teatmik Teave patsiendile Teave patsiendile Käesoleva ravimi suhtes kohaldatakse täiendavat järelevalvet, mis võimaldab kiiresti tuvastada uut ohutusteavet. Te saate sellele kaasa
CML and Fertility Leaflet EE
 VILJAKUS, PERE- PLANEERIMINE JA NOOR TÄISKASVANU MILLEGA TULEB ARVESTADA ENNE PEREKONNA LOOMIST? 2 KUI MA OLEN KMLi DIAGNOOSIGA MEES, SIIS KAS PEAKSIN SEOSES LAPSE EOSTAMISEGA MILLEGI PÄRAST MURET TUNDMA?
VILJAKUS, PERE- PLANEERIMINE JA NOOR TÄISKASVANU MILLEGA TULEB ARVESTADA ENNE PEREKONNA LOOMIST? 2 KUI MA OLEN KMLi DIAGNOOSIGA MEES, SIIS KAS PEAKSIN SEOSES LAPSE EOSTAMISEGA MILLEGI PÄRAST MURET TUNDMA?
Versioon 2.0 TEAVE ARSTIDELE BOSENTAN NORAMEDA 62,5 MG JA 125 MG ÕHUKESE POLÜMEERIKATTEGA TABLETTIDE KOHTA Enne Bosentan Norameda väljakirjutamist pat
 TEAVE ARSTIDELE BOSENTAN NORAMEDA 62,5 MG JA 125 MG ÕHUKESE POLÜMEERIKATTEGA TABLETTIDE KOHTA Enne Bosentan Norameda väljakirjutamist patsiendile, lugege palun hoolikalt ravimi omaduste kokkuvõtet. Kui
TEAVE ARSTIDELE BOSENTAN NORAMEDA 62,5 MG JA 125 MG ÕHUKESE POLÜMEERIKATTEGA TABLETTIDE KOHTA Enne Bosentan Norameda väljakirjutamist patsiendile, lugege palun hoolikalt ravimi omaduste kokkuvõtet. Kui
Microsoft PowerPoint - Kliiniliste auditite kogemused [Read-Only] [Compatibility Mode]
![Microsoft PowerPoint - Kliiniliste auditite kogemused [Read-Only] [Compatibility Mode] Microsoft PowerPoint - Kliiniliste auditite kogemused [Read-Only] [Compatibility Mode]](/thumbs/102/156360636.jpg) Anneli Rätsep TÜ Peremeditsiini õppetool vanemteadur 25.04.2013 Alates 2002. aastast "Haigete ravi pikkuse põhjendatus sisehaiguste profiiliga osakondades 3-5 auditit aastas Müokardiinfarkti haige käsitlus
Anneli Rätsep TÜ Peremeditsiini õppetool vanemteadur 25.04.2013 Alates 2002. aastast "Haigete ravi pikkuse põhjendatus sisehaiguste profiiliga osakondades 3-5 auditit aastas Müokardiinfarkti haige käsitlus
propofol: CMDh scientific conclusions and grounds for the variation, amendments to the product information and timetable for the implementation - PSUS
 I lisa Teaduslikud järeldused ja müügilubade tingimuste muutmise alused 1 Teaduslikud järeldused Võttes arvesse ravimiohutuse riskihindamise komitee hindamisaruannet propofooli perioodiliste ohutusaruannete
I lisa Teaduslikud järeldused ja müügilubade tingimuste muutmise alused 1 Teaduslikud järeldused Võttes arvesse ravimiohutuse riskihindamise komitee hindamisaruannet propofooli perioodiliste ohutusaruannete
KUI PATSIENT VAJAB KODUÕDE
 KUI PATSIENT VAJAB KODUÕDE ILVE-TEISI REMMEL JUHATAJA OÜ KODUÕDE KODUÕENDUS (HOME NURSING CARE) - KVALIFITSEERITUD ÕENDUSTEENUS, MIDA OSUTATAKSE ÄGEDA HAIGUSE PARANEMISPERIOODIS OLEVA, KROONILIST HAIGUST
KUI PATSIENT VAJAB KODUÕDE ILVE-TEISI REMMEL JUHATAJA OÜ KODUÕDE KODUÕENDUS (HOME NURSING CARE) - KVALIFITSEERITUD ÕENDUSTEENUS, MIDA OSUTATAKSE ÄGEDA HAIGUSE PARANEMISPERIOODIS OLEVA, KROONILIST HAIGUST
Dr Maire Kuddu - Keda ohustab pea ja kaelapiirkonna vähk
 Keda ohustab pea ja kaela piirkonna vähk? Maire Kuddu Põhja-Eesti Regionaalhaigla Onkoloogia-hematoloogia kliinik kiiritusravi keskus 12.10.2015 Pea ja kaela pahaloomulised kasvajad (PKK) Maailmas > 650,000
Keda ohustab pea ja kaela piirkonna vähk? Maire Kuddu Põhja-Eesti Regionaalhaigla Onkoloogia-hematoloogia kliinik kiiritusravi keskus 12.10.2015 Pea ja kaela pahaloomulised kasvajad (PKK) Maailmas > 650,000
TAI programm „Tervem ja kainem Eesti“ SA PERH Psühhiaatriakliinikus
 Kainem ja tervem Eesti (KTE) programm SA PERH psühhiaatriakliinikus Eerik Kesküla Teenusele pöördumine Saatekirjata Registreerumine tel 6172545 ja e-mail KTE@regionaalhaigla.ee Esmane hindamine 3 tööpäeva
Kainem ja tervem Eesti (KTE) programm SA PERH psühhiaatriakliinikus Eerik Kesküla Teenusele pöördumine Saatekirjata Registreerumine tel 6172545 ja e-mail KTE@regionaalhaigla.ee Esmane hindamine 3 tööpäeva
Tulemas
 Eesti Arstide Päevad 2010 25.03.2010-26.03.2010 Konverentsi teemad 25. märtsil Sarnased kaebused, erinevad haigused Sellel sessioonil püüame lahti harutada kaks teemaderingi. Krooniline obstruktiivne kopsuhaigus
Eesti Arstide Päevad 2010 25.03.2010-26.03.2010 Konverentsi teemad 25. märtsil Sarnased kaebused, erinevad haigused Sellel sessioonil püüame lahti harutada kaks teemaderingi. Krooniline obstruktiivne kopsuhaigus
IDA-TALLINNA KESKHAIGLA Statsionaarsete patsientide rahulolu uuring
 IDA-TALLINNA KESKHAIGLA Statsionaarsete patsientide rahulolu uuring 2015 2015 Sisukord: Statsionaarsete patsientide rahulolu uuring 2015... 1 1. Uuringu läbiviimise metoodika... 3 2. Andmete analüüs...
IDA-TALLINNA KESKHAIGLA Statsionaarsete patsientide rahulolu uuring 2015 2015 Sisukord: Statsionaarsete patsientide rahulolu uuring 2015... 1 1. Uuringu läbiviimise metoodika... 3 2. Andmete analüüs...
Luuravi
 Luuravi 10.01.2015 Edward Laane Multiipelne müeloom (MM) Pahaloomuline vereloome kasvaja, luuüdis paljunevad klonaalsed pahaloomulised plasmarakud ehk müeloomirakud Hüperkaltseemia (C) Neerupuudulikkus(R)
Luuravi 10.01.2015 Edward Laane Multiipelne müeloom (MM) Pahaloomuline vereloome kasvaja, luuüdis paljunevad klonaalsed pahaloomulised plasmarakud ehk müeloomirakud Hüperkaltseemia (C) Neerupuudulikkus(R)
Vähi läbilöögivalu Teave tervishoiutöötajale
 Vähi läbilöögivalu Teave tervishoiutöötajale Vähi läbilöögivalu (vllv) on mitmekesine 1 Valu on kõige sagedasem sümptom, mida seostatakse vähkkasvajaga või selle raviga. 2 Enamikul vähipatsientidest esineb
Vähi läbilöögivalu Teave tervishoiutöötajale Vähi läbilöögivalu (vllv) on mitmekesine 1 Valu on kõige sagedasem sümptom, mida seostatakse vähkkasvajaga või selle raviga. 2 Enamikul vähipatsientidest esineb
Microsoft Word - Document in Unnamed
 RAVIMI OMADUSTE KOKKUVÕTE 1. RAVIMPREPARAADI NIMETUS Roferon-A, 3 miljonit rahvusvahelist ühikut (RÜ), süstelahus süstlis 2. KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS Iga süstel sisaldab 3 miljonit rahvusvahelist
RAVIMI OMADUSTE KOKKUVÕTE 1. RAVIMPREPARAADI NIMETUS Roferon-A, 3 miljonit rahvusvahelist ühikut (RÜ), süstelahus süstlis 2. KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS Iga süstel sisaldab 3 miljonit rahvusvahelist
Untitled-1
 TERVISHOIUTÖÖTAJATE INFOLEHT MITTE- ONKOLOOGILISTE NÄIDUSTUSTE KORRAL OLULINE TEAVE RIXATHON I (rituksimab) KOHTA XXX XX.XX.2018 Teave, mis aitab tervishoiutöötajatel hoolitseda patsientide eest, kes saavad
TERVISHOIUTÖÖTAJATE INFOLEHT MITTE- ONKOLOOGILISTE NÄIDUSTUSTE KORRAL OLULINE TEAVE RIXATHON I (rituksimab) KOHTA XXX XX.XX.2018 Teave, mis aitab tervishoiutöötajatel hoolitseda patsientide eest, kes saavad
Tervishoiu ressursside kasutamine haiglavõrgu arengukava haiglates
 Tervishoiu ressursside kasutamine haiglavõrgu arengukava haiglates Tervise Arengu Instituut Tervisestatistika osakond Tervishoiu ressursside kasutamine haiglavõrgu arengukava haiglates Tallinn 2016 Tervisestatistika
Tervishoiu ressursside kasutamine haiglavõrgu arengukava haiglates Tervise Arengu Instituut Tervisestatistika osakond Tervishoiu ressursside kasutamine haiglavõrgu arengukava haiglates Tallinn 2016 Tervisestatistika
Microsoft Word - Document in Unnamed
 RAVIMI OMADUSTE KOKKUVÕTE 1. RAVIMPREPARAADI NIMETUS Nizoral, 2% kreem 2. KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS Üks gramm kreemi sisaldab 20 mg ketokonasooli. INN. Ketoconazolum Abiainete täielik loetelu
RAVIMI OMADUSTE KOKKUVÕTE 1. RAVIMPREPARAADI NIMETUS Nizoral, 2% kreem 2. KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS Üks gramm kreemi sisaldab 20 mg ketokonasooli. INN. Ketoconazolum Abiainete täielik loetelu
Abiarstide tagasiside 2016 Küsimustikule vastas 137 tudengit, kellest 81 (60%) olid V kursuse ning 56 (40%) VI kursuse tudengid. Abiarstina olid vasta
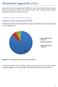 Abiarstide tagasiside 2016 Küsimustikule vastas 137 tudengit, kellest 81 (60%) olid V kursuse ning 56 (40%) VI kursuse tudengid. Abiarstina olid vastanutest töötanud 87 tudengit ehk 64%, kellest 79 (91%)
Abiarstide tagasiside 2016 Küsimustikule vastas 137 tudengit, kellest 81 (60%) olid V kursuse ning 56 (40%) VI kursuse tudengid. Abiarstina olid vastanutest töötanud 87 tudengit ehk 64%, kellest 79 (91%)
Tõenduspõhine hindamine kellele ja milleks? KIRSTI AKKERMANN TÜ PSÜHHOLOOGIA INSTITUUT KOGNITIIVSE JA KÄITUMISTERAAPIA KESKUS
 Tõenduspõhine hindamine kellele ja milleks? KIRSTI AKKERMANN TÜ PSÜHHOLOOGIA INSTITUUT KOGNITIIVSE JA KÄITUMISTERAAPIA KESKUS Tõenduspõhine praktika 2 Teadlik, läbimõeldud ja mõistlik olemasolevate teaduslikult
Tõenduspõhine hindamine kellele ja milleks? KIRSTI AKKERMANN TÜ PSÜHHOLOOGIA INSTITUUT KOGNITIIVSE JA KÄITUMISTERAAPIA KESKUS Tõenduspõhine praktika 2 Teadlik, läbimõeldud ja mõistlik olemasolevate teaduslikult
Praks 1
 Biomeetria praks 6 Illustreeritud (mittetäielik) tööjuhend Eeltöö 1. Avage MS Excel is oma kursuse ankeedivastuseid sisaldav andmestik, 2. lisage uus tööleht, nimetage see ümber leheküljeks Praks6 ja 3.
Biomeetria praks 6 Illustreeritud (mittetäielik) tööjuhend Eeltöö 1. Avage MS Excel is oma kursuse ankeedivastuseid sisaldav andmestik, 2. lisage uus tööleht, nimetage see ümber leheküljeks Praks6 ja 3.
KINNITATUD programmi nõukogu koosolekul Haridus ja Teadusministeeriumi teadus- ja arendustegevuse programmi Eesti keel ja kultuur digiajast
 KINNITATUD programmi nõukogu koosolekul 28.06.2019 Haridus ja Teadusministeeriumi teadus- ja arendustegevuse programmi Eesti keel ja kultuur digiajastul 2019-2027 projekti- ja tegevustoetuste taotlemise
KINNITATUD programmi nõukogu koosolekul 28.06.2019 Haridus ja Teadusministeeriumi teadus- ja arendustegevuse programmi Eesti keel ja kultuur digiajastul 2019-2027 projekti- ja tegevustoetuste taotlemise
Tobramycin Art 29(4)
 II lisa Teaduslikud järeldused ja positiivse arvamuse alused 3 Teaduslikud järeldused Tobramycin VVB ja sarnaste nimetuste (vt I lisa) teadusliku hindamise üldkokkuvõte Sissejuhatus UAB VVB esitas 2. mail
II lisa Teaduslikud järeldused ja positiivse arvamuse alused 3 Teaduslikud järeldused Tobramycin VVB ja sarnaste nimetuste (vt I lisa) teadusliku hindamise üldkokkuvõte Sissejuhatus UAB VVB esitas 2. mail
Microsoft Word - Document in Unnamed
 Pakendi infoleht: informatsioon kasutajale Duphalac 667 mg/ml suukaudne lahus Lactulosum Enne ravimi võtmist lugege hoolikalt infolehte, sest siin on teile vajalikku teavet. Võtke seda ravimit alati täpselt
Pakendi infoleht: informatsioon kasutajale Duphalac 667 mg/ml suukaudne lahus Lactulosum Enne ravimi võtmist lugege hoolikalt infolehte, sest siin on teile vajalikku teavet. Võtke seda ravimit alati täpselt
Soliris, INN-eculizumab
 I LISA 0BRAVIMI OMADUSTE KOKKUVÕTE 1 1. RAVIMPREPARAADI NIMETUS Soliris 300 mg infusioonilahuse kontsentraat 2. KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS Ekulizumab on NS0-rakuliinis rekombinant-dna-tehnikaga
I LISA 0BRAVIMI OMADUSTE KOKKUVÕTE 1 1. RAVIMPREPARAADI NIMETUS Soliris 300 mg infusioonilahuse kontsentraat 2. KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS Ekulizumab on NS0-rakuliinis rekombinant-dna-tehnikaga
MÄÄRUS nr 18 Välisvärbamise toetuse taotlemise ja kasutamise tingimused ning kord Määrus kehtestatakse riigieelarve seaduse 53 1 lõike 1 al
 MÄÄRUS 19.04.2018 nr 18 Välisvärbamise toetuse taotlemise ja kasutamise tingimused ning kord Määrus kehtestatakse riigieelarve seaduse 53 1 lõike 1 alusel. 1. peatükk Üldsätted 1. Välisvärbamise toetuse
MÄÄRUS 19.04.2018 nr 18 Välisvärbamise toetuse taotlemise ja kasutamise tingimused ning kord Määrus kehtestatakse riigieelarve seaduse 53 1 lõike 1 alusel. 1. peatükk Üldsätted 1. Välisvärbamise toetuse
1
 IDA-TALLINNA KESKHAIGLA Statsionaarsete patsientide rahulolu uuring 13 13 Sisukord 1. Uuringu läbiviimise metoodika... 2 2. Andmete analüüs... 2 3. Uuringu valim... 3 3.1. Vastanute iseloomustus: sugu,
IDA-TALLINNA KESKHAIGLA Statsionaarsete patsientide rahulolu uuring 13 13 Sisukord 1. Uuringu läbiviimise metoodika... 2 2. Andmete analüüs... 2 3. Uuringu valim... 3 3.1. Vastanute iseloomustus: sugu,
VL1_praks6_2010k
 Biomeetria praks 6 Illustreeritud (mittetäielik) tööjuhend Eeltöö 1. Avage MS Excel is oma kursuse ankeedivastuseid sisaldav andmestik, 2. lisage uus tööleht (Insert / Lisa -> Worksheet / Tööleht), nimetage
Biomeetria praks 6 Illustreeritud (mittetäielik) tööjuhend Eeltöö 1. Avage MS Excel is oma kursuse ankeedivastuseid sisaldav andmestik, 2. lisage uus tööleht (Insert / Lisa -> Worksheet / Tööleht), nimetage
Tallinna patsient valikute ristmikul
 Tallinna patsient valikute ristmikul Dr. Vassili Novak Konverents õpitud abitus 27 märts 2013 kiirabi 20613 80787 muul viisil saabunud 60174 25,52% 74,48% LV1 LV2 LV3 LV4 EMO saal + isolaatorid IR saal
Tallinna patsient valikute ristmikul Dr. Vassili Novak Konverents õpitud abitus 27 märts 2013 kiirabi 20613 80787 muul viisil saabunud 60174 25,52% 74,48% LV1 LV2 LV3 LV4 EMO saal + isolaatorid IR saal
Lp Armin Lastovets Rahandusministeerium Suur-Ameerika 1 Teie: nr / Tallinn Meie: a nr 5-1-4/ Edastat
 Lp Armin Lastovets Rahandusministeerium Suur-Ameerika 1 Teie: 17.09.2012 nr 12.2-1/13528 15006 Tallinn Meie: 22.02.2013.a nr 5-1-4/12-0010-146 Edastatud elektrooniliselt e-posti aadressile madli.juhani@fin.ee
Lp Armin Lastovets Rahandusministeerium Suur-Ameerika 1 Teie: 17.09.2012 nr 12.2-1/13528 15006 Tallinn Meie: 22.02.2013.a nr 5-1-4/12-0010-146 Edastatud elektrooniliselt e-posti aadressile madli.juhani@fin.ee
Dr Vahur Valvere - Konverentsi avaettekanne
 HARVA ESINEVAD ONKOLOOGILISED JA HEMATOLOOGILISED KASVAJAD TÄISKASVANUTEL JA LASTEL Vahur Valvere, MD, PhD SA PERH Onkoloogia- ja hematoloogiakliinik Eesti Vähiliit PROGRAMM Eesti Vähiliidu teaduskonverents
HARVA ESINEVAD ONKOLOOGILISED JA HEMATOLOOGILISED KASVAJAD TÄISKASVANUTEL JA LASTEL Vahur Valvere, MD, PhD SA PERH Onkoloogia- ja hematoloogiakliinik Eesti Vähiliit PROGRAMM Eesti Vähiliidu teaduskonverents
Metoodika kirjeldus 2015
 Metoodika kirjeldus 2016 Tervishoiutöötajatele ja -organisatsioonidele tasude maksmise avalikustamise aruande lisadokument Takeda Pharma AS Väljaandmise kuupäev: 01.06.2017 Metoodika kirjeldus 2016 1.
Metoodika kirjeldus 2016 Tervishoiutöötajatele ja -organisatsioonidele tasude maksmise avalikustamise aruande lisadokument Takeda Pharma AS Väljaandmise kuupäev: 01.06.2017 Metoodika kirjeldus 2016 1.
MAJANDUSAASTA ARUANNE aruandeaasta algus: aruandeaasta lõpp: ärinimi: Osaühing Puka Vesi registrikood: tänava/talu nimi
 MAJANDUSAASTA ARUANNE aruandeaasta algus: 01.01.2016 aruandeaasta lõpp: 31.12.2016 ärinimi: registrikood: 12548743 tänava/talu nimi, Kooli tn 6 maja ja korteri number: alevik: Puka alevik vald: Puka vald
MAJANDUSAASTA ARUANNE aruandeaasta algus: 01.01.2016 aruandeaasta lõpp: 31.12.2016 ärinimi: registrikood: 12548743 tänava/talu nimi, Kooli tn 6 maja ja korteri number: alevik: Puka alevik vald: Puka vald
Maris Jesse 2017_06_09_EHL_konverents_
 Lähiaja tervishoiupoliitilised muutused Sotsiaalministeerium 6.09.2017 1. Tervishoiu rahastamine 2. Muudatused Eesti Haigekassa juhtimises 3. Muudatused täiendavas ravimihüvitises Haigekassast tasutud
Lähiaja tervishoiupoliitilised muutused Sotsiaalministeerium 6.09.2017 1. Tervishoiu rahastamine 2. Muudatused Eesti Haigekassa juhtimises 3. Muudatused täiendavas ravimihüvitises Haigekassast tasutud
Praks 1
 Biomeetria praks 6 Illustreeritud (mittetäielik) tööjuhend Eeltöö 1. Avage MS Excel is ankeedivastuseid sisaldav andmestik, 2. lisage uus tööleht, nimetage see ümber leheküljeks Praks6 ja 3. kopeerige
Biomeetria praks 6 Illustreeritud (mittetäielik) tööjuhend Eeltöö 1. Avage MS Excel is ankeedivastuseid sisaldav andmestik, 2. lisage uus tööleht, nimetage see ümber leheküljeks Praks6 ja 3. kopeerige
HÜPER IGM SÜNDROOM Publikatsioon oli võimalik tänu CSL Behring üldisele koolitusgrantile
 HÜPER IGM SÜNDROOM Publikatsioon oli võimalik tänu CSL Behring üldisele koolitusgrantile HÜPER IGM SÜNDROOM See brosüür on ette nähtud patsientidele ja nende perekondadele ja ei asenda kliinilise immunoloogi
HÜPER IGM SÜNDROOM Publikatsioon oli võimalik tänu CSL Behring üldisele koolitusgrantile HÜPER IGM SÜNDROOM See brosüür on ette nähtud patsientidele ja nende perekondadele ja ei asenda kliinilise immunoloogi
ET I LISA KOONDDOKUMENT NIMETUS KPN/KGT-XX-XXXX Taotluse esitamise kuupäev: XX-XX-XXXX 1. REGISTREERITAV(AD) NIMETUS(ED) KOLMAS RIIK, KUHU MÄÄRA
 ET I LISA KOONDDOKUMENT NIMETUS KPN/KGT-XX-XXXX Taotluse esitamise kuupäev: XX-XX-XXXX 1. REGISTREERITAV(AD) NIMETUS(ED) 2. KOLMAS RIIK, KUHU MÄÄRATLETUD PIIRKOND KUULUB: 3. GEOGRAAFILISE TÄHISE TÜÜP:
ET I LISA KOONDDOKUMENT NIMETUS KPN/KGT-XX-XXXX Taotluse esitamise kuupäev: XX-XX-XXXX 1. REGISTREERITAV(AD) NIMETUS(ED) 2. KOLMAS RIIK, KUHU MÄÄRATLETUD PIIRKOND KUULUB: 3. GEOGRAAFILISE TÄHISE TÜÜP:
Kyprolis, INN-carfilzomib
 I LISA RAVIMI OMADUSTE KOKKUVÕTE 1 Käesoleva ravimi suhtes kohaldatakse täiendavat järelevalvet, mis võimaldab kiiresti tuvastada uut ohutusteavet. Tervishoiutöötajatel palutakse teavitada kõigist võimalikest
I LISA RAVIMI OMADUSTE KOKKUVÕTE 1 Käesoleva ravimi suhtes kohaldatakse täiendavat järelevalvet, mis võimaldab kiiresti tuvastada uut ohutusteavet. Tervishoiutöötajatel palutakse teavitada kõigist võimalikest
Sissejuhatus GRADE metoodikasse
 Sissejuhatus GRADE metoodikasse Eriline tänu: Holger Schünemann ja GRADE working group www.gradeworkinggroup.org Kaja-Triin Laisaar TÜ peremeditsiini ja rahvatervishoiu instituut kaja-triin.laisaar@ut.ee
Sissejuhatus GRADE metoodikasse Eriline tänu: Holger Schünemann ja GRADE working group www.gradeworkinggroup.org Kaja-Triin Laisaar TÜ peremeditsiini ja rahvatervishoiu instituut kaja-triin.laisaar@ut.ee
M16 Final Decision_Recalculation of MTR for EMT
 1 OTSUS Tallinn 22.juuni 2007 J.1-45/07/7 Mobiiltelefonivõrgus häälkõne lõpetamise hinnakohustuse kehtestamine AS EMT- le Sideameti 21. märtsi 2006. a otsusega nr J.1-50/06/2 tunnistati AS EMT (edaspidi
1 OTSUS Tallinn 22.juuni 2007 J.1-45/07/7 Mobiiltelefonivõrgus häälkõne lõpetamise hinnakohustuse kehtestamine AS EMT- le Sideameti 21. märtsi 2006. a otsusega nr J.1-50/06/2 tunnistati AS EMT (edaspidi
EVL tegevus 2013
 Eesti Vähiliidu 2013 aasta tegevusaruanne Vähiregistri andmetel elab Eestis ligikaudu 45 000 vähipatsienti (seisuga 2008) igal aastal tuleb juurde umbes 7122 esmajuhtu ja sureb ca 3600 haiget. Viimase
Eesti Vähiliidu 2013 aasta tegevusaruanne Vähiregistri andmetel elab Eestis ligikaudu 45 000 vähipatsienti (seisuga 2008) igal aastal tuleb juurde umbes 7122 esmajuhtu ja sureb ca 3600 haiget. Viimase
Söömishäired lastel ja noortel
 Söömishäired lastel ja noortel Ere Vasli Lastepsühhiaater SA Tallinna Lastehaigla/ Laste Vaimse Tervise Keskus 24.aprill 2014.a. Söömishäired laste ja noortel Terve ja patoloogiline söömiskäitumine Söömishäired
Söömishäired lastel ja noortel Ere Vasli Lastepsühhiaater SA Tallinna Lastehaigla/ Laste Vaimse Tervise Keskus 24.aprill 2014.a. Söömishäired laste ja noortel Terve ja patoloogiline söömiskäitumine Söömishäired
AJOVY, INN-fremanezumab
 I LISA RAVIMI OMADUSTE KOKKUVÕTE 1 Käesoleva ravimi suhtes kohaldatakse täiendavat järelevalvet, mis võimaldab kiiresti tuvastada uut ohutusteavet. Tervishoiutöötajatel palutakse teavitada kõigist võimalikest
I LISA RAVIMI OMADUSTE KOKKUVÕTE 1 Käesoleva ravimi suhtes kohaldatakse täiendavat järelevalvet, mis võimaldab kiiresti tuvastada uut ohutusteavet. Tervishoiutöötajatel palutakse teavitada kõigist võimalikest
Rahulolu_uuring_2010.pdf
 Rahulolu raport Kuressaare Haigla SA Käesolev uuring viidi läbi 2010. aastal. Uuriti ambulatoorse ravi patsientide rahulolu raviteenusega. Ankeetide arv ja tagastusprotsent Struktuuriüksus Väljastatud
Rahulolu raport Kuressaare Haigla SA Käesolev uuring viidi läbi 2010. aastal. Uuriti ambulatoorse ravi patsientide rahulolu raviteenusega. Ankeetide arv ja tagastusprotsent Struktuuriüksus Väljastatud
Lasteendokrinoloogia aktuaalsed küsimused
 Haigusjuht nooruki androloogiast lasteendokrinoloogi pilgu läbi Aleksandr Peet SA TÜK Lastekliinik aleksandr.peet@kliinikum.ee Neuroloogi jälgimisel vanuseni 13 a. Esmakordselt visiidil vanuses 7a Elu
Haigusjuht nooruki androloogiast lasteendokrinoloogi pilgu läbi Aleksandr Peet SA TÜK Lastekliinik aleksandr.peet@kliinikum.ee Neuroloogi jälgimisel vanuseni 13 a. Esmakordselt visiidil vanuses 7a Elu
Slide 1
 Ravimite soodusnimekirja lisamise protsess 14.11.2012 Päevakava 9.00 9.15 Hommikukohv ja registreerumine 9.15 9.30 Sissejuhatus (moderaator Ain Aaviksoo) 9.30 9.55 Priit Kruus tutvustab uuringu tulemusi
Ravimite soodusnimekirja lisamise protsess 14.11.2012 Päevakava 9.00 9.15 Hommikukohv ja registreerumine 9.15 9.30 Sissejuhatus (moderaator Ain Aaviksoo) 9.30 9.55 Priit Kruus tutvustab uuringu tulemusi
Microsoft Word - Document in Unnamed
 Pakendi infoleht: teave kasutajale Octenisept 1 mg/ 20 mg/ml, nahalahus Oktenidiindivesinikkloriid Fenoksüetanool Enne ravimi kasutamist lugege hoolikalt infolehte, sest siin on teile vajalikku teavet.
Pakendi infoleht: teave kasutajale Octenisept 1 mg/ 20 mg/ml, nahalahus Oktenidiindivesinikkloriid Fenoksüetanool Enne ravimi kasutamist lugege hoolikalt infolehte, sest siin on teile vajalikku teavet.
Sepsise ravijuhend
 Ravijuhendi Sepsise ja septilise šoki esmane diagnostika ja ravi koosoleku protokoll nr 3 Kuupäev Koht Osalesid Puudusid Juhataja 12.mai 2017, 12.00-15.00 Tartu, Ravila 19, ruum 1038 Joel Starkopf (juht),
Ravijuhendi Sepsise ja septilise šoki esmane diagnostika ja ravi koosoleku protokoll nr 3 Kuupäev Koht Osalesid Puudusid Juhataja 12.mai 2017, 12.00-15.00 Tartu, Ravila 19, ruum 1038 Joel Starkopf (juht),
Microsoft Word - Document in Unnamed
 RAVIMI OMADUSTE KOKKUVÕTE 1. RAVIMPREPARAADI NIMETUS Terbinafin-ratiopharm, 10 mg/g kreem 2. KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS 1 g kreemi sisaldab 10 mg terbinafiinvesinikkloriidi. INN. Terbinafinum
RAVIMI OMADUSTE KOKKUVÕTE 1. RAVIMPREPARAADI NIMETUS Terbinafin-ratiopharm, 10 mg/g kreem 2. KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS 1 g kreemi sisaldab 10 mg terbinafiinvesinikkloriidi. INN. Terbinafinum
Iluteenused_A5.indd
 Tarbija meelespea KASUTA TARGALT! KOSMEETIKATOODETE kasutamise eesmärk on inimese keha kaitsmine, muutmine, heas seisus hoidmine või lõhnastamine. Enne järjekordse kosmeetikatoote ostmist anname sulle
Tarbija meelespea KASUTA TARGALT! KOSMEETIKATOODETE kasutamise eesmärk on inimese keha kaitsmine, muutmine, heas seisus hoidmine või lõhnastamine. Enne järjekordse kosmeetikatoote ostmist anname sulle
Lisa 2 Kinnitatud Kambja Vallavalitsuse määrusega nr 11 PUUDEGA LAPSE HOOLDUS- JA SOTSIAALTEENUSTE VAJADUSE HINDAMISVAHEND Lapsevaema/hoold
 Lisa 2 Kinnitatud Kambja Vallavalitsuse 08.03.2018 määrusega nr 11 PUUDEGA LAPSE HOOLDUS- JA SOTSIAALTEENUSTE VAJADUSE HINDAMISVAHEND Lapsevaema/hooldaja/kontaktisiku üldandmed Ees ja perekonnanimi Isikukood
Lisa 2 Kinnitatud Kambja Vallavalitsuse 08.03.2018 määrusega nr 11 PUUDEGA LAPSE HOOLDUS- JA SOTSIAALTEENUSTE VAJADUSE HINDAMISVAHEND Lapsevaema/hooldaja/kontaktisiku üldandmed Ees ja perekonnanimi Isikukood
Microsoft Word - Document in Unnamed
 Pakendi infoleht: teave kasutajale OFTAQUIX 5 mg/ml silmatilgad, lahus Levofloksatsiin Enne ravimi kasutamist lugege hoolikalt infolehte, sest siin on teile vajalikku teavet. - Hoidke infoleht alles, et
Pakendi infoleht: teave kasutajale OFTAQUIX 5 mg/ml silmatilgad, lahus Levofloksatsiin Enne ravimi kasutamist lugege hoolikalt infolehte, sest siin on teile vajalikku teavet. - Hoidke infoleht alles, et
Microsoft Word - Uudiskirja_Toimetulekutoetus docx
 Toimetulekutoetuse maksmine 2014. 2018. aastal Sotsiaalministeeriumi analüüsi ja statistika osakond Toimetulekutoetust on õigus saada üksi elaval isikul või perekonnal, kelle kuu netosissetulek pärast
Toimetulekutoetuse maksmine 2014. 2018. aastal Sotsiaalministeeriumi analüüsi ja statistika osakond Toimetulekutoetust on õigus saada üksi elaval isikul või perekonnal, kelle kuu netosissetulek pärast
ITK ettekande põhi
 Kodade virvendusarütmia antitrombootiline ravi Heli Kaljusaar 2009 NB! Loeng on autori omand ja kaitstud autoriõiguse seadusega. Loengut võite kasutada isiklikukeks vajadusteks. Loengu reprodutseerimisel
Kodade virvendusarütmia antitrombootiline ravi Heli Kaljusaar 2009 NB! Loeng on autori omand ja kaitstud autoriõiguse seadusega. Loengut võite kasutada isiklikukeks vajadusteks. Loengu reprodutseerimisel
VME_Toimetuleku_piirmäärad
 Tapa TAPA VALLAVOLIKOGU MÄÄRUS EELNÕU 30. aprill 2015 nr Eluruumi alaliste kulude piirmäärade kehtestamine toimetulekutoetuse määramisel Määrus kehtestatakse kohaliku omavalitsuse korralduse seaduse 22
Tapa TAPA VALLAVOLIKOGU MÄÄRUS EELNÕU 30. aprill 2015 nr Eluruumi alaliste kulude piirmäärade kehtestamine toimetulekutoetuse määramisel Määrus kehtestatakse kohaliku omavalitsuse korralduse seaduse 22
liigtarvitamine_A5.indd
 ALKOHOLI LIIGTARVITAMINE MIS SEE ON JA KUST SAAB ABI Hoiad käes vihikut, mis räägib alkoholi liigtarvitamisest. Seda lugedes saad ülevaate sellest, mis on alkoholi liigtarvitamine, mida tähendab alkoholitarvitamise
ALKOHOLI LIIGTARVITAMINE MIS SEE ON JA KUST SAAB ABI Hoiad käes vihikut, mis räägib alkoholi liigtarvitamisest. Seda lugedes saad ülevaate sellest, mis on alkoholi liigtarvitamine, mida tähendab alkoholitarvitamise
Spinraza, INN-nusinersen
 I LISA RAVIMI OMADUSTE KOKKUVÕTE 1 Käesoleva ravimi suhtes kohaldatakse täiendavat järelevalvet, mis võimaldab kiiresti tuvastada uut ohutusteavet. Tervishoiutöötajatel palutakse teavitada kõigist võimalikest
I LISA RAVIMI OMADUSTE KOKKUVÕTE 1 Käesoleva ravimi suhtes kohaldatakse täiendavat järelevalvet, mis võimaldab kiiresti tuvastada uut ohutusteavet. Tervishoiutöötajatel palutakse teavitada kõigist võimalikest
Tervise- ja tööministri a määrusega nr 41 kinnitatud Töölesaamist toetavad teenused lisa 1 vorm A Sihtasutus Innove Lõõtsa Tallinn
 Tervise- ja tööministri 11.09.2015. a määrusega nr 41 kinnitatud Töölesaamist toetavad teenused lisa 1 vorm A Sihtasutus Innove Lõõtsa 4 11415 Tallinn Meetme 3.2 Tööturuteenused tagamaks paremaid võimalusi
Tervise- ja tööministri 11.09.2015. a määrusega nr 41 kinnitatud Töölesaamist toetavad teenused lisa 1 vorm A Sihtasutus Innove Lõõtsa 4 11415 Tallinn Meetme 3.2 Tööturuteenused tagamaks paremaid võimalusi
M16 Final Decision_Recalculation of MTR for Elisa
 OTSUS Tallinn 20.06.2007 J.1-45/07/4 Mobiiltelefonivõrgus häälkõne lõpetamise hinnakohustuse kehtestamine Elisa Eesti AS- le Sideameti 21. märtsi 2006. a otsusega nr J.1-50/06/2 tunnistati AS EMT (edaspidi
OTSUS Tallinn 20.06.2007 J.1-45/07/4 Mobiiltelefonivõrgus häälkõne lõpetamise hinnakohustuse kehtestamine Elisa Eesti AS- le Sideameti 21. märtsi 2006. a otsusega nr J.1-50/06/2 tunnistati AS EMT (edaspidi
Non-pharmacological treatment
 Kroonilise sageduskontrolli ravim Kliiniline küsimus Kas kroonilise sageduskontrolli strateegia puhul tuleks kodade virvendusarütmia patsientidel esmavalikuna eelistada BBL vs KKB vs muid ravimeid? Olulised
Kroonilise sageduskontrolli ravim Kliiniline küsimus Kas kroonilise sageduskontrolli strateegia puhul tuleks kodade virvendusarütmia patsientidel esmavalikuna eelistada BBL vs KKB vs muid ravimeid? Olulised
Lisa 1 I Üldsätted 1. Riigihanke korraldamisel tuleb tagada rahaliste vahendite läbipaistev, otstarbekas ja säästlik kasutamine, isikute võrdne kohtle
 Lisa 1 I Üldsätted 1. korraldamisel tuleb tagada rahaliste vahendite läbipaistev, otstarbekas ja säästlik kasutamine, isikute võrdne kohtlemine ning olemasolevate konkurentsitingimuste efektiivne ärakasutamine.
Lisa 1 I Üldsätted 1. korraldamisel tuleb tagada rahaliste vahendite läbipaistev, otstarbekas ja säästlik kasutamine, isikute võrdne kohtlemine ning olemasolevate konkurentsitingimuste efektiivne ärakasutamine.
Microsoft Word - Document in Unnamed
 PAKENDI INFOLEHT: INFORMATSIOON KASUTAJALE (käsimüügiravim*) IMODIUM, 2 mg kõvakapslid Loperamiidvesinikkloriid Lugege infolehte hoolikalt, sest siin on teile vajalikku teavet. Ehkki seda ravimit on võimalik
PAKENDI INFOLEHT: INFORMATSIOON KASUTAJALE (käsimüügiravim*) IMODIUM, 2 mg kõvakapslid Loperamiidvesinikkloriid Lugege infolehte hoolikalt, sest siin on teile vajalikku teavet. Ehkki seda ravimit on võimalik
Endokrinoloogia eriala arengukava aastani
 Endokrinoloogia eriala arengukava aastani 2020 2012 Koostajad: Ülle Jakovlev, Ida-Tallinna Keskhaigla Eve Kelk, Ida-Tallinna Keskhaigla Maire Lubi, TÜ Kliinikum Tarvo Rajasalu, TÜ Kliinikum Vallo Volke,
Endokrinoloogia eriala arengukava aastani 2020 2012 Koostajad: Ülle Jakovlev, Ida-Tallinna Keskhaigla Eve Kelk, Ida-Tallinna Keskhaigla Maire Lubi, TÜ Kliinikum Tarvo Rajasalu, TÜ Kliinikum Vallo Volke,
EMA_2011_ _ET_TRA
 II LISA Euroopa Ravimiameti esitatud teaduslikud järeldused ning positiivse arvamuse alused 1 Teaduslikud järeldused Docetaxel Teva Genrics ja sarnaste nimetuste (vt I lisa) teadusliku hindamise üldkokkuvõte
II LISA Euroopa Ravimiameti esitatud teaduslikud järeldused ning positiivse arvamuse alused 1 Teaduslikud järeldused Docetaxel Teva Genrics ja sarnaste nimetuste (vt I lisa) teadusliku hindamise üldkokkuvõte
Microsoft Word - alkohol_K2_SoKo.doc
 Soovituste koostamise kokkuvõte - SoKo Kliiniline küsimus nr 2 Kas kõigil alkoholi kuritarvitamise ja alkoholisõltuvuse kahtlusega patsientidel tuleb lisaks anamneesile kasutada diagnoosi täpsustamiseks
Soovituste koostamise kokkuvõte - SoKo Kliiniline küsimus nr 2 Kas kõigil alkoholi kuritarvitamise ja alkoholisõltuvuse kahtlusega patsientidel tuleb lisaks anamneesile kasutada diagnoosi täpsustamiseks
raamat5_2013.pdf
 Peatükk 5 Prognoosiintervall ja Usaldusintervall 5.1 Prognoosiintervall Unustame hetkeks populatsiooni parameetrite hindamise ja pöördume tagasi üksikvaatluste juurde. On raske ennustada, milline on huvipakkuva
Peatükk 5 Prognoosiintervall ja Usaldusintervall 5.1 Prognoosiintervall Unustame hetkeks populatsiooni parameetrite hindamise ja pöördume tagasi üksikvaatluste juurde. On raske ennustada, milline on huvipakkuva
Soodustuste nimekiri
 Tervise- ja tööministri 29. detsembri 2016. a määruse nr 82 "Sotsiaalministri 24. septembri 2002. a määruse nr 112 "Eesti Haigekassa ravimite loetelu" muutmine" lisa Sotsiaalministri 24. septembri 2002.
Tervise- ja tööministri 29. detsembri 2016. a määruse nr 82 "Sotsiaalministri 24. septembri 2002. a määruse nr 112 "Eesti Haigekassa ravimite loetelu" muutmine" lisa Sotsiaalministri 24. septembri 2002.
Kodusünnitus Eestis miks, kuidas, millal? Siiri Põllumaa RM, MSc Eesti Ämmaemandate Ühing EAL, 3.aprill 2014
 Kodusünnitus Eestis miks, kuidas, millal? Siiri Põllumaa RM, MSc Eesti Ämmaemandate Ühing EAL, 3.aprill 2014 Teema on reguleerimata (13-aastane ajalugu) tundlik Propaganda, PR? Lubada või keelata? õigus
Kodusünnitus Eestis miks, kuidas, millal? Siiri Põllumaa RM, MSc Eesti Ämmaemandate Ühing EAL, 3.aprill 2014 Teema on reguleerimata (13-aastane ajalugu) tundlik Propaganda, PR? Lubada või keelata? õigus
EMA ENET
 II lisa Teaduslikud järeldused ja positiivse arvamuse alused 5 Teaduslikud järeldused Ravimi Valebo ja sarnaste nimetuste (vt I lisa) teadusliku hindamise üldkokkuvõte Taustteave Valebo on kombinatsioonpakend,
II lisa Teaduslikud järeldused ja positiivse arvamuse alused 5 Teaduslikud järeldused Ravimi Valebo ja sarnaste nimetuste (vt I lisa) teadusliku hindamise üldkokkuvõte Taustteave Valebo on kombinatsioonpakend,
Microsoft PowerPoint - BPP_MLHvaade_juuni2012 (2)
 Balti pakendi protseduur MLH kogemus Iivi Ammon, Ravimitootjate Liit Ravimiameti infopäev 13.06.2012 Eeltöö ja protseduuri algus Päev -30 MLH esindajad kolmes riigis jõuavad arusaamani Balti pakendi protseduuri
Balti pakendi protseduur MLH kogemus Iivi Ammon, Ravimitootjate Liit Ravimiameti infopäev 13.06.2012 Eeltöö ja protseduuri algus Päev -30 MLH esindajad kolmes riigis jõuavad arusaamani Balti pakendi protseduuri
PowerPointi esitlus
 Eesti Haigekassa töökorralduse muudatustest ja EPIKoja esindamisest Ulvi Tammer-Jäätes EPIK juhatuse liige Eesti Haigekassa Nõukogu liige EHK Soodusravimikomisjoni liige Eesti Diabeediliidu juhataja Organisatsioon
Eesti Haigekassa töökorralduse muudatustest ja EPIKoja esindamisest Ulvi Tammer-Jäätes EPIK juhatuse liige Eesti Haigekassa Nõukogu liige EHK Soodusravimikomisjoni liige Eesti Diabeediliidu juhataja Organisatsioon
Kuidas, kus ja milleks me kujundame poliitikaid Kuidas mõjutavad meid poliitikad ja instrumendid Euroopa Liidu ja riigi tasandil Heli Laarmann Sotsiaa
 Kuidas, kus ja milleks me kujundame poliitikaid Kuidas mõjutavad meid poliitikad ja instrumendid Euroopa Liidu ja riigi tasandil Heli Laarmann Sotsiaalministeerium Rahvatervise osakond 15.06.2018 Mis on
Kuidas, kus ja milleks me kujundame poliitikaid Kuidas mõjutavad meid poliitikad ja instrumendid Euroopa Liidu ja riigi tasandil Heli Laarmann Sotsiaalministeerium Rahvatervise osakond 15.06.2018 Mis on
Microsoft Word - Document in Unnamed
 Pakendi infoleht: teave kasutajale Betaserc 8 mg tabletid Betaserc 16 mg tabletid Betaserc 24 mg tabletid Beetahistiindivesinikkloriid Enne ravimi kasutamist lugege hoolikalt infolehte, sest siin on teile
Pakendi infoleht: teave kasutajale Betaserc 8 mg tabletid Betaserc 16 mg tabletid Betaserc 24 mg tabletid Beetahistiindivesinikkloriid Enne ravimi kasutamist lugege hoolikalt infolehte, sest siin on teile
Zevalin, INN-Ibritumomab tiuxetan
 I LISA RAVIMI OMADUSTE KOKKUVÕTE 1 1. RAVIMPREPARAADI NIMETUS Zevalin, 1,6 mg/ml radiofarmatseutiline komplekt infusiooniks 2. KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS Zevalin i turustatakse komplektidena
I LISA RAVIMI OMADUSTE KOKKUVÕTE 1 1. RAVIMPREPARAADI NIMETUS Zevalin, 1,6 mg/ml radiofarmatseutiline komplekt infusiooniks 2. KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS Zevalin i turustatakse komplektidena
(Microsoft Word - Matsalu Veev\344rk AS aktsion\344ride leping \(Lisa D\) Valemid )
 1(6) 1. Vee- ja kanalisatsiooniteenuse hinna kujundamise põhimõtted Aktsiaselts tegevuskulude arvestuse aluseks on auditeeritud ja kinnitatud aastaaruanne. Hinnakujunduse analüüsis kasutatakse Aktsiaseltsi
1(6) 1. Vee- ja kanalisatsiooniteenuse hinna kujundamise põhimõtted Aktsiaselts tegevuskulude arvestuse aluseks on auditeeritud ja kinnitatud aastaaruanne. Hinnakujunduse analüüsis kasutatakse Aktsiaseltsi
TAI_meta_99x148_EST.indd
 METADOONASENDUSRAVI Narkootikumide süstimine seab Sind ohtu nakatuda HI- või hepatiidiviirusega, haigestuda südamehaigustesse (nt endokardiit) või põdeda muid haigusi. Kuna narkootikumide süstimine on
METADOONASENDUSRAVI Narkootikumide süstimine seab Sind ohtu nakatuda HI- või hepatiidiviirusega, haigestuda südamehaigustesse (nt endokardiit) või põdeda muid haigusi. Kuna narkootikumide süstimine on
Soodustuste nimekiri
 Sotsiaalministri 24. septembri 2002. a määruse nr 112 "Eesti Haigekassa ravimite loetelu" lisa EESTI HAIGEKASSA RAVIMITE LOETELU 1539547 abirateroon, 2mg L02BX03 ZYTIGA, tablett, 120TK JANSSEN-CILAG INTERNATIONAL
Sotsiaalministri 24. septembri 2002. a määruse nr 112 "Eesti Haigekassa ravimite loetelu" lisa EESTI HAIGEKASSA RAVIMITE LOETELU 1539547 abirateroon, 2mg L02BX03 ZYTIGA, tablett, 120TK JANSSEN-CILAG INTERNATIONAL
Soodustuste nimekiri
 Sotsiaalministri 24. septembri 2002. a määruse nr 112 "Eesti Haigekassa ravimite loetelu" lisa EESTI HAIGEKASSA RAVIMITE LOETELU 1539547 abirateroon, 2mg L02BX03 ZYTIGA, tablett, 120TK JANSSEN-CILAG INTERNATIONAL
Sotsiaalministri 24. septembri 2002. a määruse nr 112 "Eesti Haigekassa ravimite loetelu" lisa EESTI HAIGEKASSA RAVIMITE LOETELU 1539547 abirateroon, 2mg L02BX03 ZYTIGA, tablett, 120TK JANSSEN-CILAG INTERNATIONAL
EELNÕU TÕRVA LINNAVOLIKOGU MÄÄRUS Tõrva 15.märts 2016 nr. Koduteenuste loetelu ning nende osutamise tingimused ja kord Määrus kehtestatakse kohaliku o
 EELNÕU TÕRVA LINNAVOLIKOGU MÄÄRUS Tõrva 15.märts 2016 nr. Koduteenuste loetelu ning nende osutamise tingimused ja kord Määrus kehtestatakse kohaliku omavalitsuse korralduse seaduse 22 lg 1 p 5 ja sotsiaalhoolekande
EELNÕU TÕRVA LINNAVOLIKOGU MÄÄRUS Tõrva 15.märts 2016 nr. Koduteenuste loetelu ning nende osutamise tingimused ja kord Määrus kehtestatakse kohaliku omavalitsuse korralduse seaduse 22 lg 1 p 5 ja sotsiaalhoolekande
IGA ravitulemuse saavutamine ON PÕHJUS TÄHISTAMISEKS Varajase ja olulise molekulaarse ravivastuse saavutamine tähendab seda, et teie Ph+ KML allub rav
 IGA ravitulemuse saavutamine ON PÕHJUS TÄHISTAMISEKS Varajase ja olulise molekulaarse ravivastuse saavutamine tähendab seda, et teie Ph+ KML allub ravile. 1-3 Vaadake, mida saate oma järgmise ravivastuse
IGA ravitulemuse saavutamine ON PÕHJUS TÄHISTAMISEKS Varajase ja olulise molekulaarse ravivastuse saavutamine tähendab seda, et teie Ph+ KML allub ravile. 1-3 Vaadake, mida saate oma järgmise ravivastuse
EA0911.indd
 Päriliku rinna- ja munasarjavähiga patsientide geneetilise konsulteerimise ja jälgimise juhend Tiiu-Liis Tigane¹, Piret Laidre², Kairit Joost³, Neeme Tõnisson²,⁴, Valdur Mikita⁵, Katrin Õunap²,⁶, Riina
Päriliku rinna- ja munasarjavähiga patsientide geneetilise konsulteerimise ja jälgimise juhend Tiiu-Liis Tigane¹, Piret Laidre², Kairit Joost³, Neeme Tõnisson²,⁴, Valdur Mikita⁵, Katrin Õunap²,⁶, Riina
Väljaandja: Põllumajandusminister Akti liik: määrus Teksti liik: algtekst-terviktekst Redaktsiooni jõustumise kp: Redaktsiooni kehtivuse lõ
 Väljaandja: Põllumajandusminister Akti liik: määrus Teksti liik: algtekst-terviktekst Redaktsiooni jõustumise kp: 17.06.2011 Redaktsiooni kehtivuse lõpp: 17.05.2013 Avaldamismärge: RT I, 14.06.2011, 1
Väljaandja: Põllumajandusminister Akti liik: määrus Teksti liik: algtekst-terviktekst Redaktsiooni jõustumise kp: 17.06.2011 Redaktsiooni kehtivuse lõpp: 17.05.2013 Avaldamismärge: RT I, 14.06.2011, 1
bioenergia M Lisa 2.rtf
 Põllumajandusministri 20. juuli 2010. a määruse nr 80 «Bioenergia tootmise investeeringutoetuse saamise nõuded, toetuse taotlemise ja taotluse menetlemise täpsem kord» lisa 2 Tabel 1 Taotleja andmed 1.1
Põllumajandusministri 20. juuli 2010. a määruse nr 80 «Bioenergia tootmise investeeringutoetuse saamise nõuded, toetuse taotlemise ja taotluse menetlemise täpsem kord» lisa 2 Tabel 1 Taotleja andmed 1.1
AASTAARUANNE
 2014. 2018. aasta statistikatööde loetelu kinnitamisel juunis 2014 andis Vabariigi Valitsus Statistikaametile ja Rahandusle korralduse (valitsuse istungi protokolliline otsus) vaadata koostöös dega üle
2014. 2018. aasta statistikatööde loetelu kinnitamisel juunis 2014 andis Vabariigi Valitsus Statistikaametile ja Rahandusle korralduse (valitsuse istungi protokolliline otsus) vaadata koostöös dega üle
Praks 1
 Biomeetria praks 3 Illustreeritud (mittetäielik) tööjuhend Eeltöö 1. Avage MS Excel is oma kursuse ankeedivastuseid sisaldav andmestik, 2. lisage uus tööleht, 3. nimetage see ümber leheküljeks Praks3 ja
Biomeetria praks 3 Illustreeritud (mittetäielik) tööjuhend Eeltöö 1. Avage MS Excel is oma kursuse ankeedivastuseid sisaldav andmestik, 2. lisage uus tööleht, 3. nimetage see ümber leheküljeks Praks3 ja
Microsoft Word - RVLi juhend.doc
 KINNITATUD peadirektori 23. mai 2008.a käskkirjaga nr 32 I. ÜLDSÄTTED EESTI RAHVUSRAAMATUKOGU RAAMATUKOGUDEVAHELISE LAENUTUSE JUHEND 1. Käesolev juhend sätestab raamatukogudevahelise laenutuse (edaspidi
KINNITATUD peadirektori 23. mai 2008.a käskkirjaga nr 32 I. ÜLDSÄTTED EESTI RAHVUSRAAMATUKOGU RAAMATUKOGUDEVAHELISE LAENUTUSE JUHEND 1. Käesolev juhend sätestab raamatukogudevahelise laenutuse (edaspidi
Kinnitatud Setomaa Liidu üldkoosolekul Setomaa edendüsfond 1. SEF eesmärk MTÜ Setomaa Liit juures asuv Setomaa edendüsfond (SEF) on loodud
 Kinnitatud Setomaa Liidu üldkoosolekul 29.11.2018 Setomaa edendüsfond 1. SEF eesmärk MTÜ Setomaa Liit juures asuv Setomaa edendüsfond (SEF) on loodud rahaliste vahendite sihipärase kogumiseks ja sihtotstarbelise
Kinnitatud Setomaa Liidu üldkoosolekul 29.11.2018 Setomaa edendüsfond 1. SEF eesmärk MTÜ Setomaa Liit juures asuv Setomaa edendüsfond (SEF) on loodud rahaliste vahendite sihipärase kogumiseks ja sihtotstarbelise
struktuuriüksus
 Haigla Tähis THA/46 Viide KHA/2 Versioon 1 TEAVIK Klienditeeninduse standard lisa 8 SA VILJANDI HAIGLA ISIKUANDMETE TÖÖTLEMISE PÕHIMÕTTED SISSEJUHATUS Sihtasutus Viljandi Haigla (registrikood 90004585,
Haigla Tähis THA/46 Viide KHA/2 Versioon 1 TEAVIK Klienditeeninduse standard lisa 8 SA VILJANDI HAIGLA ISIKUANDMETE TÖÖTLEMISE PÕHIMÕTTED SISSEJUHATUS Sihtasutus Viljandi Haigla (registrikood 90004585,
HINDAMISKRITEERIUMID 2013 Põhja-Harju Koostöökogule esitatud projektide hindamine toimub vastavalt hindamise töökorrale, mis on kinnitatud 24.okt.2012
 HINDAMISKRITEERIUMID 01 Põhja-Harju Koostöökogule esitatud projektide hindamine toimub vastavalt hindamise töökorrale, mis on kinnitatud.okt.01 üldkoosoleku otsuega nr (Lisa ) Hindamiskriteeriumid on avalikud
HINDAMISKRITEERIUMID 01 Põhja-Harju Koostöökogule esitatud projektide hindamine toimub vastavalt hindamise töökorrale, mis on kinnitatud.okt.01 üldkoosoleku otsuega nr (Lisa ) Hindamiskriteeriumid on avalikud
Microsoft Word - VOTA_dok_menetlemine_OIS_ doc
 Varasemate õpingute ja töökogemuse arvestamine (VÕTA ) dokumentide menetlemise protsess ÕISis Koostanud: Ele Hansen Ele Mägi Tartu 2012 1. Aine ülekandmine-õppekavajärgne aine Varasemalt sooritatud aine
Varasemate õpingute ja töökogemuse arvestamine (VÕTA ) dokumentide menetlemise protsess ÕISis Koostanud: Ele Hansen Ele Mägi Tartu 2012 1. Aine ülekandmine-õppekavajärgne aine Varasemalt sooritatud aine
No Slide Title
 Eutanaasia. Arsti pilk Katrin Elmet katrin.elmet@kliinikum.ee 24. november 2010 Eutanaasia surma saabumise Aktiivne eutanaasia Passiivne eutanaasia kiirendamine Soovitud (voluntary) Soovimatu (non-voluntary)
Eutanaasia. Arsti pilk Katrin Elmet katrin.elmet@kliinikum.ee 24. november 2010 Eutanaasia surma saabumise Aktiivne eutanaasia Passiivne eutanaasia kiirendamine Soovitud (voluntary) Soovimatu (non-voluntary)
(Microsoft Word - ÜP küsimustiku kokkuvõte kevad 2019)
 Ümbrikupalkade küsimustiku kokkuvõte Ülevaade on koostatud alates 2017. aasta kevadest korraldatud küsitluste põhjal, võimalusel on võrdlusesse lisatud ka 2016. aasta küsitluse tulemused, kui vastava aasta
Ümbrikupalkade küsimustiku kokkuvõte Ülevaade on koostatud alates 2017. aasta kevadest korraldatud küsitluste põhjal, võimalusel on võrdlusesse lisatud ka 2016. aasta küsitluse tulemused, kui vastava aasta
Microsoft Word - essee_CVE ___KASVANDIK_MARKKO.docx
 Tartu Ülikool CVE-2013-7040 Referaat aines Andmeturve Autor: Markko Kasvandik Juhendaja : Meelis Roos Tartu 2015 1.CVE 2013 7040 olemus. CVE 2013 7040 sisu seisneb krüptograafilises nõrkuses. Turvaaugu
Tartu Ülikool CVE-2013-7040 Referaat aines Andmeturve Autor: Markko Kasvandik Juhendaja : Meelis Roos Tartu 2015 1.CVE 2013 7040 olemus. CVE 2013 7040 sisu seisneb krüptograafilises nõrkuses. Turvaaugu
